X’e bağlı Retinoskizis ve Güncel Tedavisi
Okuma:4198
X’e bağlı retinoskizis (XLRS), retinoskizin proteinini kodlayan RS1 genindeki mutasyon sonucu oluşan, nadir görülen kalıtsal bir hastalıktır. Retinoskizin proteini, retinada birçok hücre yüzeyine güçlü ve spesifik bir şekilde bağlanan, fotoreseptörler ve bipolar hücreler tarafından salgılanıp eksprese edilen yapısal bir proteindir. Retinoskizinin mutant formları ile uygun şekilde bağlanma oluşamadığından, retina tabakalarında ayrılma ve skizis ile karşılaşılmaktadır. XLRS’nin ABD ve Avrupa’da tahmini prevelansı 35,000 olup, erkeklerde insidansın 1/5000-1/20000 aralığında olduğu varsayılmaktadır. XLRS li hastalar için günümüzde hala onaylanmış tedaviler bulunmamaktadır.
X’e bağlı Retinoskiziste Klinik Özellikler
XLRS,RS1 geninde mutasyonu olan bireylerde tam penetrans göstermekle birlikte, aynı aileden etkilenmiş üyelerin arasında bile santral görme kaybı ve retinoskizisin ciddiyetine bağlı olarak fenotip ekspresyonu açısından yüksek çeşitlilik görülmektedir.
Klasik olarak; XLRS, okul çağında, foveal retinoskizis ve 20/60 ile 20/120 aralığında azalmış görme keskinliği ile ortaya çıkar. Bazı vakalarda, retina dekolmanı veya vitreus hemorajisi gibi eşlik eden komplikasyonlar varlığında XLRS daha erken olarak infant döneminde de saptanabilmektedir. XLRS, her ne kadar bilateral olarak görülse de, asimetrisite ve sekonder komplikasyonlara bağlı olarak iki göz arasında eşit olmayan görme kaybı da ortaya çıkabilir.
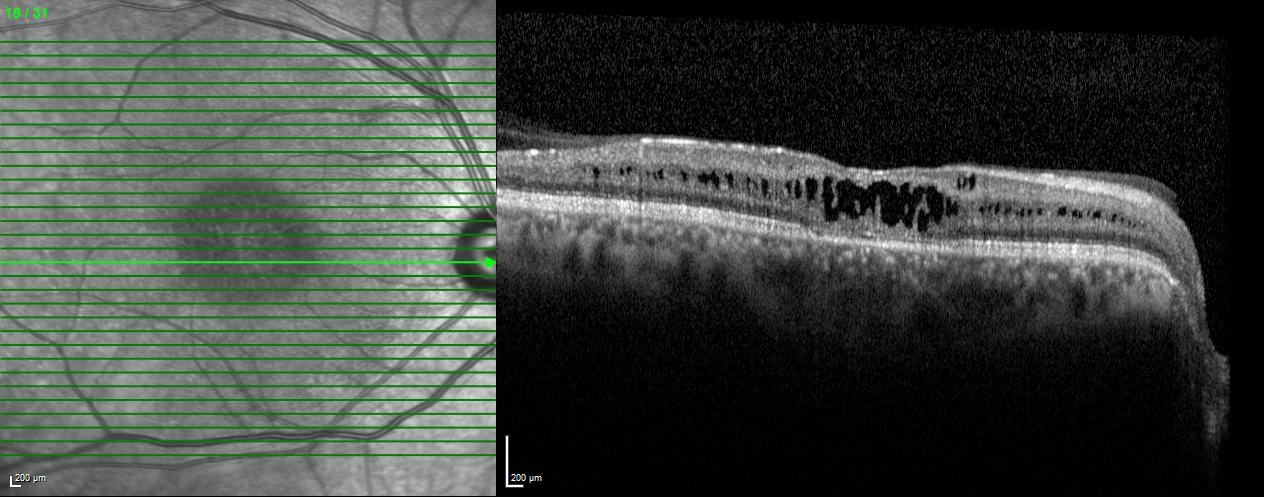
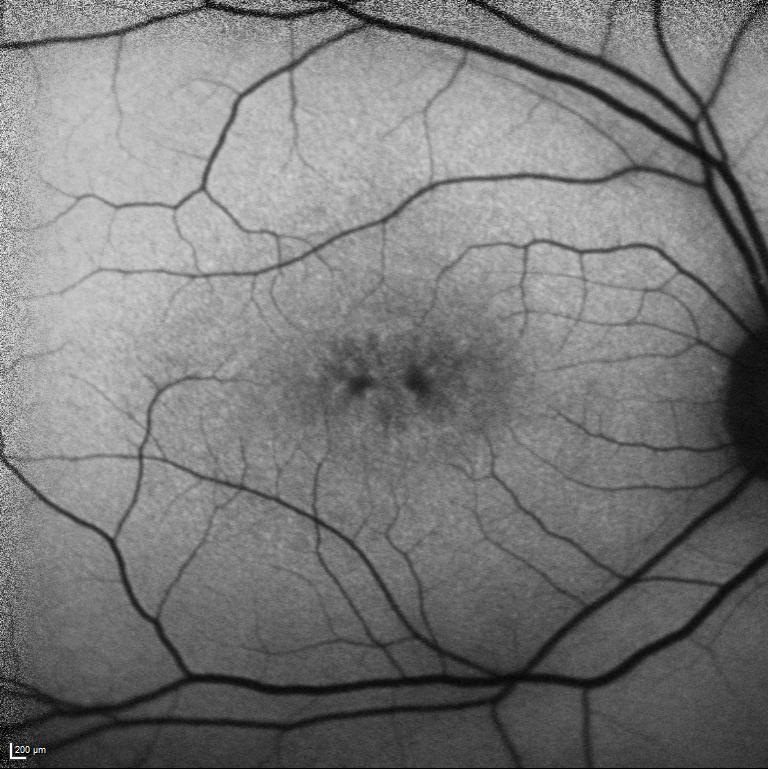
Neredeyse tüm XLRS hastalarında maküloskizis veya maküla tabakalarında ayrılma görülmektedir. Bu durum fundus oftalmoskopide makülada karakteristik bisiklet jantının tellerine benzeyen görüntü ile tanınmaktadır. Bazı vakalarda, hipopigmentasyona veya maküloskizisin neden olduğu bal peteği görünümüne rastlanabilmektedir.
Görüntüleme
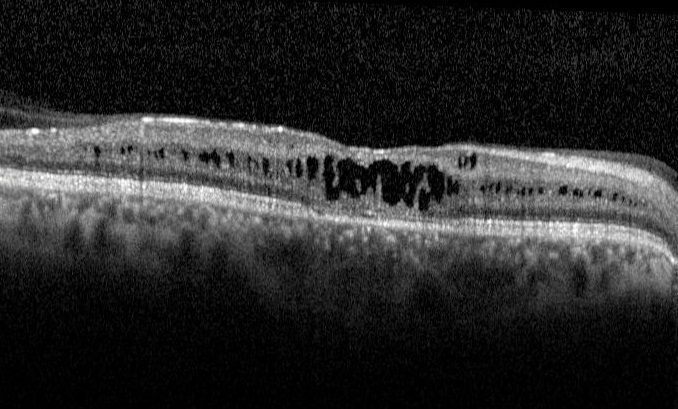
OCT ile alınan görüntüler, XLRS hastalarında, retina tabakalarındaki düzensizlik ve ayrışmayı desteklemektedir. Retinal kalınlık, skizis kavitelerinin varlığına bağlı olarak genellikle artmıştır. OCT çalışmaları, retinanın birden çok tabakasında –retina sinir lifi tabakası, iç nükleer tabaka, dış nükleer tabaka, dış plexiform tabaka- ayrışmaların olabileceğini göstermiştir.
Makuloskizis, foveaya yerleşmiş olabileceği gibi para foveal alana da sınırlanmış olabilir. Tüm hastalarda maküloskizise rastlanırken hastaların yaklaşık yarısında ayrıca periferal retinoskizis saptanır.
ERG: XLRS hastalarının yaklaşık yarısında tam alan ERG testinde karakteristik bir bozukluk gözlenir. Bu testte; skotopik durumda parlak ışıkla uyarılma sonucu b/a dalga amplitüd oranının 1 den küçük olduğu negatif bir dalga formu oluşur. XLRS hastalarındaki negatif dalga formu yanıtının yapısı ve ciddiyetinin hasta yaşı ve RS1 genindeki hastalık oluşturan mutasyonun ciddiyeti ile korele olduğu öne sürülmüştür.
XLRS de hastalık progresyonu ile ilgili çalışmalar devam etmektedir. Bazı çalışmalar moleküler patolojide ve görsel semptomlarda zaman içinde tanı konduğu andaki duruma göre belirgin bir kötüleşme olmadığını vurgulamaktadır. Bazı çalışmalarda ise, yaşa bağlı olarak moleküler morfolojide belirgin değişiklikler olabileceği belirtilmiştir. Genç XLRS hastalarının retina içi skizis kaviteleri nedeniyle daha kalın retinaya sahip oldukları, daha ileri yaş XLRS hastalarının ise düzleşme ve kollaps nedeniyle daha ince retinaya sahip oldukları tanımlanmıştır.
Günümüzde XLRS de hastalığın ilerleyişini belirlemek amacıyla biri The National Eye Institute diğeri ise Applied Genetic Technologies Corporation tarafından olmak üzere iki çalışma yürütülmektedir.
,
X’e bağlı Retinoskiziste Moleküler Özellikler
RS1 geni, X kromozomunun kısa kolunda yer alan, 32.4 kb uzunluğunda bir gendir. RS1 geninin kodlamış olduğu 24 kDa lık retinoskizin peptidi, 224 aminoasit içermekte ve ekstraselüler boşluğa salınmadan önce homo-octamer hale dönüşmektedir.
Hastalığın % 40 kadarında nonsense veya frameshift mutasyonları sonucu oluşan RS1 ilişkili varyantlar, normal uzunluktaki retinoskizin peptidi oluşmasına engel olmaktadır. Oluşan bu kısa peptidler de hücre tarafından hızlıca parçalara ayrıştırılabilen, stabil olmayan özellik göstermektedirler. Hastalığın % 50 den fazlasında ise, yanlış anlamlı değişimlerin sebep olduğu RS1 mutasyon u sonucu uzunluğu normal olmakla beraber anormal peptid üretimi söz konusudur.
Retinoskizin peptidi; bir N-terminal lider sekansı, RS1 alanı, diskoid alan ve C-terminal segmentten oluşmuştur. XLRS hastalarında bu bölümlerden herhangi birinde mutasyon bulunabilmektedir.
Tedavi İçin Yeni Geliştirilen Seçenekler
XLR hastaları için herhangi bir onaylanmış tedavi seçeneği bulunmamaktadır. Bu hastalarda görsel iyileştirme için, büyük metinli, yüksek kontrastlı okuma materyalleri tavsiye edilmektedir.
Bazı çalışmalarda, dorzolamide gibi karbonik anhidraz inhibitörlerinin skizis derecesinde azalmayı sağlayabileceği gösterilse de bu raporların çoğu olgu sunumu veya retrospektif vaka çalışmalarına dayanmaktadır.
Bir prospektif randomize klinik çalışmada, 3 aylık oral asetozolamid tedavisi sonrası 11 hastanın 6 sında en iyi düzeltilmiş görme keskinliğinde 0,1 logMAR (5 ETDRS harfi) düzeyine artış sağlandığı ancak skizis derecesindeki değişikliklerle korelasyon saptanmadığı belirtilmiştir.
Gen Tedavisi: XLRS hastaları için gen tedavisi yeni geliştirilen bir tedavi seçeneğidir. İnsan RS1 geni sentezleyen adeno-ilişkili viral (adeno-associated viral -AAV) vektörlerin kullanılması klinik olarak geliştirilme aşamasındadır.
Gen tedavisi, genetik defekti tamir etmek için, sıklıkla viral vektörlerin kullanıldığı hastanın kendi hücresine işlevsel bir gen örneğinin verilmesi esasına dayanır. Böylece hastalığın altta yatan sebebini çözerek hastalığın yol açtığı problemlerde düzelme sağlanır.
AAV, retinal hastalıkların gen tedavisi için uygun hale getirilmiş, sadece zayıf bir immün cevap oluşturan ve insanda hastalık yapıcı bir özelliği saptanmamış olan basit, küçük, zarfsız, nonpatojenik bir virüstür. Gen tedavisine uyarlamak için, AAV vektörlerinden iki doğal viral gen çıkarılıp yerine tedavi edici protein kodlayan insan geni konulmaktadır. AAV vektörleri başka viral gen içermediğinden, viral genlerin yaratabileceği yan etkiler ortadan kalkmış olmaktadır. XLRS tedavisine yönelik gen çalışmalarının potansiyel tedavi edici etkisini araştırmak üzere yürütülen preklinik çalışmalar, özellikle hayvan modellerinde RS1 ekspresyonu sağlayan AAV vektörlerinin potansiyel güvenlik ve etkinliğini araştırmak üzerine yoğunlaşmıştır.
XLRS li bir fare modelinde, fare veya insan RS1 ini eksprese eden AAV vektörlerinin subretinal veya intravitreal enjeksiyonları sonrası, retinal hücre tabakalarında düzen sağlandığı ve ERG de skotopik şartlar altında elde edilen b dalgasında düzelme sağlandığı görülmüştür.
Tavşanlar, primatları içeren büyük memelilere ait güvenlik çalışmalarında, insan RS1 ini eksprese eden AAV vektörlerinin intravitreal enjeksiyonlarının güvenli olduğu fakat doz bağımlı olarak kendi kendini sınırlayan ön ve arka segment inflamasyonuna yol açabileceği belirtilmiştir.
AAV ile ilgili klinik denemeler
Bu ve diğer preklinik çalışmalar XLRS deki gen tedavisinin klinik gelişimini desteklemektedir. Denemeler XLRS li hastalarda insan RS 1 ini eksprese eden AAV vektörlerinin intravitreal enjeksiyonlarının tolerabilite ve güvenliğini araştırmak üzerine yoğunlaşmıştır.
NCI tek merkezli, randomize olmayan, doz artımına yönelik bir deneme yürütmektedir. Katılımcılar 18 yaş ve üzeri XLRS li erkek hastalardır. Katılımcıların bir gözüne insan RSA1 ekspresyonu yapan AAV vektörü tek doz olarak uygulanmaktadır. Çalışma toplamda 15 katılımcı kayıt yaptırmış olacak şekilde iki gruba ayrılmıştır.
İlk aşamada, ilk katılımcılara düşük doz ile uygulama yapılırken takip eden hastalara daha yüksek dozda enjeksiyon içerikleri uygulanmaktadır. İkinci aşamada ise katılımcılara; ilk aşamada potansiyel olarak etkin olduğu ve iyi tolere edilebildiği saptanan dozajlar uygulanmaktadır.
Güvenlik değerlendirmeleri; yan etkiler, laboratuvar testleri, retinal fonksiyon ve oküler yapının analizini içermektedir. İkincil sonuçlar ise enjeksiyon sonrası görsel fonksiyon, ERG cevabı, OCT ile değerlendirilen retinal yapı değişiklikleri, görme alanı ölçümleri, AAV ve RS1 e olan immün cevabı kapsamaktadır.
ABD’ de dört farklı yerde çok merkezli, randomize olmayan, doz yükseltme denemeleri üzerine kurulu bir çalışma yürütülmektedir. Katılımcıların bir gözüne insan RS1 eksprese eden tek doz AAV enjeksiyonu intravitreal olarak uygulanmaktadır. Bu çalışma toplam 27 katılımcı olmak üzere iki gurupta yapılmaktadır. İlk aşamada, en düşük doz uygulaması yapılmakta, Veri ve Güvenlik İzleme Komitesinin güvenlik dataları incelendikten sonra artan dozlarda toplam üç doz uygulaması yapılmaktadır. Bu doz artımı uygulanan katılımcılar 18 yaş ve üzeri XLRS li erkek hastalardır.
İkinci guruba katılanlar 6 yaş ve üzerinde XLRS li erkek hastalardır ve bu hastalara ilk aşamada saptanan maksimum tolere edilebilen doz uygulanmaktadır. Güvenlik değerlendirmeleri, RS1 e karşı immün cevap ve yan etkilerin sayı ve oranlarını inceleyerek yapılmaktadır. Etkinlik incelemeleri ise enjeksiyon sonrası görme keskinliğindeki ve skizis kavitesindeki boyut değişikliğine bakılarak yapılmaktadır.
Sonuç
XLRS henüz kesin bir tedavisi olmayan, nadir görülen kalıtsal bir hastalıktır. Görme keskinliğindeki azalma için hâlihazırdaki önerilerimiz az görenlere yardımcı cihazlara yönlendirmekle sınırlı kalmaktadır. Genetik göz hastalıklarında görsel yetinin tekrar kazanılması üzerine yoğunlaşarak AAV gen tedavisi uygulaması geliştirilmiştir ki bu denemeler XLRS tedavisinin geleceğini belirlemektedir.
[Kaynaklar: 1- Molday RS, Kellner U, Weber BH. X-linked juvenile retinoschisis: clinical diagnosis, genetic analysis, and molecular mechanisms. Prog Retin Eye Res. 2012 May;31(3):195-212. 2- Marangoni D, Wu Z, Wiley HE, Zeiss CJ, Vijayasarathy C, Zeng Y, Hiriyanna S, Bush RA, Wei LL, Colosi P, Sieving PA. Preclinical safety evaluation of a recombinant AAV8 vector for X-linked retinoschisis after intravitreal administration in rabbits. 3- Yang P. Emerging Treatment for Xlinked Retinoschisis. Retinal Physician. 2015;12:64-68. 4- Ye GJ, Budzynski E, Sonnentag P, Miller PE, Sharma AK, Ver Hoeve JN, Howard K, Knop DR, Neuringer M, McGill T, Stoddard J, Chulay JD. Safety and Biodistribution Evaluation in Cynomolgus Macaques of rAAV2tYF-CB-hRS1, a Recombinant Adeno-Associated Virus Vector Expressing Retinoschisin. Hum Gene Ther Clin Dev. 2015 Sep;26(3):165-76.]
Not: Katkılarından dolayı Dr. Gökhan Ertuğrul ve Dr. Mehmet Çıtırık’a teşekkür ederiz.
Web sitesindeki bu bilgiyi, sunu ve yayınlarınızda aşağıdaki şekilde kaynak göstererek kullanabilirsiniz.
(Ertuğrul G, Çıtırık M, Teke MY. X’e bağlı Retinoskizis ve Güncel Tedavisi. http://www.retinaclub.com/ Son Güncellenme Tarihi 01/08/2017).